Vi hverken ser eller hører det, men overalt omkring os udkæmpes der konstant drabelige slag med nogle af verdens mest sofistikerede våben. Ja, en del af slagene udkæmpes sågar på – og inden i – os selv.
Nu er det ikke svært at gætte, at de krigsførende parter er mikroorganismer. Det, de slås om, er ikke mindst adgang til næringsstoffer. Og deres våbenarsenal består af komplekse molekyler, som gennem millioner af års evolution er forfinede med det ene formål præcist at binde sig til proteiner i konkurrerende mikroorganismer for derved at slå dem ihjel.
”Man kan kalde dem for molekylære præcisionsbomber. Og de udgør et optimalt udgangspunkt for at opdage nye behandlinger af en række sygdomme,” fortæller adjunkt Thomas Bjørnskov Poulsen fra Institut for Kemi på Aarhus Universitet.
Thomas Bjørnskov Poulsen leder en forskningsgruppe, som er lykkedes med at syntetisere en sådan præcisionsbombe i laboratoriet – nemlig cellegiften rakicidin A.
Rakicidin A produceres naturligt af bakterier af Micromonospora-familien, som heldigvis ikke hører til blandt de organismer, der udkæmper drabelige slag på eller i vore kroppe. Ikke mens vi er i live, i hvert fald. De lever nemlig af dødt organisk stof og er udbredt i jord, hav og vandløb.
Det særlige ved denne bakteries våben, cellegiften rakicidin A, er, at den målrettet angriber celler, der vokser i miljøer næsten uden ilt – såkaldte hypoxiske celler.
Det er praktisk for bakterier langt nede i jorden eller i havbunden. Men det kan også være gavnligt for mennesker på hospitalernes kræftafdelinger.
Hypoxiske celler dannes nemlig også i ondartede kræftsvulster, der typisk har dårlig iltforsyning, og de spiller en vigtig rolle i metastase, altså at få kræften til at sprede sig i kroppen. Og de er modstandsdygtige over for strålebehandling, fordi de radioaktive stråler skal bruge ilt til at danne de frie iltradikaler, som beskadiger kræftcellernes DNA. Således skal man bruge to-tre gange så kraftig stråling for at få has på det samme antal hypoxiske kræftceller som man skal bruge på normoxiske (altså normalt iltede) celler.
Videnskaben har siden 2007 vidst, at rakicidin A udvundet fra bestemte Micromonospora-bakterier kan angribe og dræbe hypoxiske kræftceller.
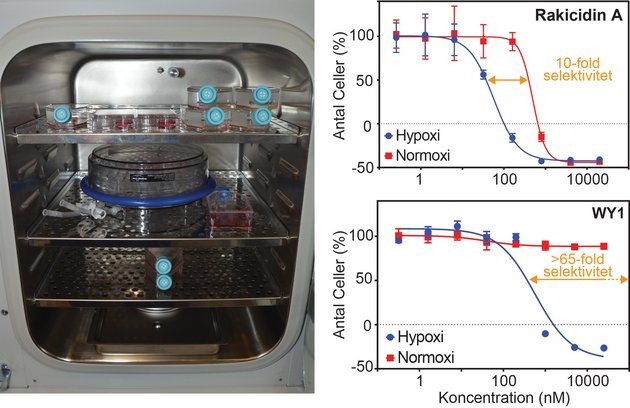
Det kan den syntetiske rakicidin A, som forskergruppen i Aarhus har skabt, også. Indledende forsøg i laboratoriet har vist, at det kunstige rakicidin A slår hypoxiske kræftceller fra bl.a. bugspytkirtelkræft ihjel, men lader normoxiske celler i fred – i hvert fald inden for en vis koncentration.
Det er en stor udfordring at fremstille et molekyle så komplekst som rakicidin A fra grunden, og de sidste fem-seks år har forskere verden over kappedes om at finde en måde at syntetisere stoffet på.
Thomas Bjørnskov Poulsen sammenligner det med at forsøge at bygge en LEGO-robot, hvor alle klodser skal sidde helt korrekt, for at robotten kan fungere, og hvor pasformen af en ny klods afhænger af hver eneste af de andre klodser, som er sat på allerede.
”Jo flere klodser, der allerede er samlet, jo sværere bliver det at sætte de næste på. Og der er ingen byggevejledning. Den skal man selv opfinde,” siger han.
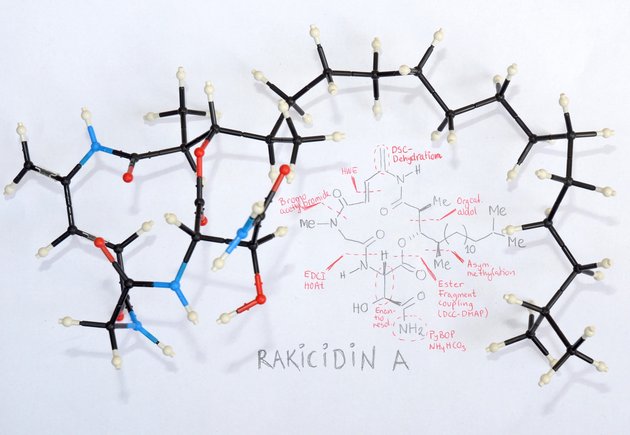
Efter at have fået adgang til syntetisk rakicidin A arbejder forskerholdet nu videre med to målsætninger:
For det første vil de finde ud af, hvordan stoffet virker – herunder nøjagtigt hvilke biomolekyler (målproteiner) rakicidin A påvirker for selektivt at kunne ramme de hypoxiske kræftceller.
”Vi har f.eks. afprøvet en række andre stoffer med kendte virkningsmekanismer, for at se om nogle af dem udviser samme “selektivitets-fingeraftryk” som rakicidin A, men vi har endnu ikke fundet et match. Og da rakicidin A strukturelt er et ganske unikt molekyle indikerer det, at dets virkningsmekanisme er ny. Når vi har klarlagt den, kan det potentielt føre til nye angrebsvinkler for kræftbehandling,” siger Thomas Bjørnskov Poulsen.
Ved at indbygge en ekstra lille kemisk markør i rakicidin A kan forskerne anvende stoffet, som så kaldes en molekylær probe, aktivt til at opdage dets målprotein. Hvis man tænker på målproteinet som en nål i en høstak bestående af tusinder af proteiner i en kræftcelle, vil den molekylære probe fungere som en magnet.
Den anden målsætning går ud på at afprøve rakicidin A i levende organismer for at afklare stoffets potentiale.
Prækliniske og evt. senere kliniske forsøg kræver betragtelige mængder af stoffet, og selvom forskerne selv kan fremstille rakicidin A, så er den strukturelle kompleksitet stadig for høj til at kunne producere større mængder.
Men da forskerne nu ligger inde med byggevejledningen, har de også forudsætningerne for at ændre og forsimple den molekylære struktur. De har allerede skabt et nyt syntetisk stof, som overordnet set har den samme struktur som rakicidin A, men hvor de har fjernet næsten alle de mest udfordrende strukturkomponenter.
Stoffet, som de kalder WY1, er en svagere cellegift end rakicidin A, men har i laboratorieeksperimenter til gengæld vist sig at gå endnu mere målrettet efter hypoxiske kræftceller, end rakicidin A gør. Det er slet ikke giftigt for kræftceller, der vokser i en atmosfære med normalt iltindhold, og den simplere struktur giver et realistisk udgangspunkt for at producere større mængder af et molekyle til præklinisk afprøvning.
Forskningen i Thomas B. Poulsens laboratorie er støttet af Lundbeckfonden, Kræftens bekæmpelse og Carlsbergfondet